Het toevoegen van de MammaPrint® aan de standaard risico-inschatting bij patiënten met vroeg-stadium borstkanker leidt niet aantoonbaar tot gezondheidswinst in vergelijking met de huidige manier waarop bepaald wordt of een patiënt chemotherapie nodig heeft. De uitkomsten van deze genetische test zijn te onzeker om vrouwen met borstkanker gefundeerd van chemotherapie te laten afzien. Het Zorginstituut keek daarvoor naar het verschil in 5 jaar overleving zonder uitzaaiingen als voorspeller voor algehele overleving na 10 jaar. Het weglaten van chemotherapie op basis van de MammaPrint® leidt mogelijk tot een toename in uitzaaiingen en daarmee sterfte. Hierdoor komt deze test niet voor vergoeding uit het basispakket in aanmerking.
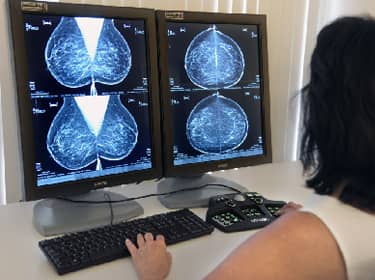
Niet afzien van chemotherapie op basis van MammaPrint®
Het Zorginstituut heeft beoordeeld of de MammaPrint® in het basispakket moet komen en heeft zich daarbij gebaseerd op de uitkomsten van de internationale MINDACT-studie, die het ‘klinisch nut’ van deze test wilde aantonen. We spreken van klinisch nut, wanneer het toevoegen van de MammaPrint®-test - en de keuze van de behandeling die daaruit volgt - leidt tot gezondheidswinst in vergelijking tot de manier waarop op dit moment bepaald wordt of een patiënt chemotherapie nodig heeft. Daarbij gaat het niet alleen om overleving, maar ook om kwaliteit van leven. Uit de studie blijkt dat na 5 jaar 94,0% van de MammaPrint®-patiënten en 96,5% van de andere patiënten nog in leven waren zonder uitzaaiingen op afstand, een verschil van gemiddeld 2,5%. Omdat er veel onzekerheid over deze gegevens bestaat, kan het in het meest ongunstige geval zelfs gaan om een verschil van 5,3%. Dit is voor het Zorginstituut een zwaarwegend argument bij de beoordeling: het weglaten van chemotherapie op basis van de MammaPrint® leidt mogelijk tot een toename in uitzaaiingen en daarmee tot sterfte.
Kans op genezing vroeg stadium borstkanker groot
Wanneer borstkanker in een vroeg stadium wordt ontdekt, is de kans op genezing groot door goede behandelmogelijkheden, waaronder chemotherapie. Het doel van chemotherapie is het voorkomen van uitgroei van eventueel aanwezige uitzaaiingen die ten tijde van de diagnose niet zichtbaar zijn. De behandeling van borstkanker hangt onder meer af van leeftijd, de grootte van de tumor, het soort borstkanker, de agressiviteit en de hormoongevoeligheid. Op basis van deze factoren bepaalt de behandelaar het risico dat een tumor mogelijk al is uitgezaaid, zonder dat dat zichtbaar is. Als de inschatting van het risico op uitzaaiing hoog is, volgt meestal chemotherapie. Chemotherapie heeft echter nare korte termijn en lange termijn bijwerkingen. Het zou dus mooi zijn als van tevoren het risico op uitzaaiingen beter ingeschat kan worden, zodat minder vrouwen de belastende chemotherapie hoeven te ondergaan. De MINDACT-studie toont echter niet aan dat op basis van de MammaPrint® chemotherapie veiliger achterwege kan worden gelaten, dan met de nu gebruikte standaardtest Adjuvant! Online (AO!). Ook behandelaren geven in hun recente richtlijn aan dat AO! dé test blijft voor het advies over het al dan niet ondergaan van chemotherapie.
Mammaprint® eerder negatief beoordeeld
De MammaPrint® is ruim 10 jaar geleden geïntroduceerd met als doel te voorspellen voor welke vrouwen chemotherapie nodig is, en voor welke niet. Waarbij de veronderstelling is dat er een groep patiënten is waarbij de voordelen van chemotherapie mogelijk niet opwegen tegen de bijwerkingen van deze therapie.
In 2010 bracht het CVZ, de voorganger van het Zorginstituut, een negatief standpunt uit over de MammaPrint®. Volgens het CVZ kon niet worden aangetoond dat het gebruik ervan gezondheidswinst oplevert ten opzichte van de standaard werkwijze. Met andere woorden: het bewijs voor klinisch nut van de test ontbrak. Daarom kwam de test ook toen al niet in het basispakket van de zorgverzekering.
Europese samenwerking: ook in ander landen niet vergoed
Het Zorginstituut heeft de MammaPrint® nu beoordeeld in samenwerking met zusterorganisaties in andere Europese landen. Het Zorginstituut en het Federaal Kenniscentrum voor de Gezondheidszorg (KCE) uit België begeleiden het onderzoek, maar ook de van overheidswege verantwoordelijke organisaties uit Frankrijk, Oostenrijk en Duitsland waren betrokken. Het rapport is in december 2017 gepubliceerd en was het uitgangspunt voor de Nederlandse beoordeling. Ook andere landen hebben op basis van het rapport nu negatief geoordeeld over de test.